Lý thuyết hóa cơ học 12
Lý thuyết hóa 12 học kì 1 đầy đủ chi tiết nhất được Vn
Doc soạn gửi tới bạn đọc là toàn thể kiến thức chất hóa học 12 kì 1 về phần hữu cơ. Nội dung được xây dựng không ngừng mở rộng theo kết cấu nội dung định hướng sách giáo khoa. Từ đó giúp chúng ta học sinh thuận lợi nắm được trọng tâm tương tự như các câu chữ ý chủ yếu của từng bài.
Bạn đang xem: Tổng hợp kiến thức hóa 12 học kì 1
Mời các bạn tham khảo tài liệu bài tập liên quan:
Lý thuyết hóa 12 chương 2: Cacbonhiđrat không thiếu thốn nhấtPolime nào sau đây được tổng hợp bởi phản ứng trùng ngưng
Bảng nhận thấy các chất hữu cơ bài bác tập tất cả đáp án
Bộ 5 đề thi học kì 1 môn hóa học lớp 12 năm học tập 2021 – 2022 bao gồm đáp án
TỔNG HỢP LÝ THUYẾT HÓA 12
Một số kỹ năng và kiến thức ôn tập trước lúc vào bài bác este
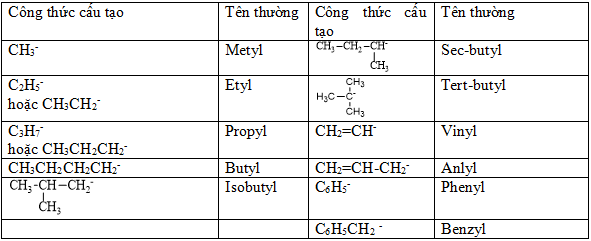
Bảng 1: tên thường gọi của một số axit thường gặp
Bảng 2: tên thường gọi của 1 số gốc thường gặp
 CHƯƠNG I : ESTE – LIPIT
CHƯƠNG I : ESTE – LIPIT

BÀI 1 : ESTE
I. Khái niệm: Khi sửa chữa nhóm OH- vào phân tử axit cacboxylic bởi nhóm OR’ của phân tử ancol, ta chiếm được este.
Ví dụ: CH3COOH + C2H5OH

Tổng quát RCOOH + R’OH

II. Đồng phân, danh pháp:
RCOOR’ (R là H hoặc cội hiđrocacbon , R’ là cội hiđrocacbon )
Cách gọi: “Tên nơi bắt đầu hiđrocacbon R’ + thương hiệu anion gốc axit (gọi theo tên thường xuyên của axit, đuôi ic => at )”
1/ Este no, 1-1 chức, mạch hở:
Cn
H2n
O2 (n ≥ 2) hoặc Cn
H2n+1COOCm
H2m+1 (n ≥ 0 , m ≥ 1)
| HCOOCH2CH2CH3 propyl fomat | isopropyl fomat | CH3COOC2H5 etyl axetat | C2H5COOCH3 metyl propionat |
n = 5 : C5H10O2 (9 este)
HCOOCH2CH2CH2CH3 butyl fomat | sec-butyl fomat | isobutyl fomat |
tert-butyl fomat | CH3COOCH2CH2CH3 propyl axetat | ispropyl axetat |
C2H5COOCH2CH3 metyl propionat | CH3CH2CH2COOCH3 metyl butirat | metyl isobutirat |
2. Este không no, 1-1 chức, mạch hở, 1 nối đôi C=C: Cn
H2n-2O2 (n ≥ 3)
+ n = 3: C3H4O2 (1 este) HCOOCH=CH2: vinyl fomat
+ n = 4: C4H6O2 (5 este)
Ngoài ra, este C4H6O4 còn đồng phân
và este C5H8O4 còn đồng phân không thuộc hai dạng phân loại ở trên.
III. Tính chất vật lí
Các este là hóa học lỏng hoặc rắn ở điều kiện thường.
Các este bám mùi thơm sệt trưng: isoamyl axetat CH3COOCH2CH2CH(CH3)2 bám mùi chuối chín, etyl butirat CH3CH2CH2COOC2H5 và etyl propionat CH3CH2COOC2H5 có mùi dứa, geranyl axetat nặng mùi hoa hồng, benzyl axetat CH3COOCH2C6H5 có mùi hoa nhài….
Không rã trong nước, nhẹ hơn nước. Thường sẽ có t0 sôi với độ tan trong nước thấp rộng hẳn các axit và ancol thuộc số cacbon hoặc cùng phân tử khối (nguyên nhân: không sinh sản được liên kết hiđrô thân este cùng với nước và este cùng với nhau).
IV. đặc thù hóa học
1/ phản ứng thủy phân: (phản ứng đặc thù của este)
a/ Thủy phân trong môi trường xung quanh axit:
Ví dụ: CH3COOC2H5 + H2O CH3COOH + C2H5OH
Tổng quát: RCOOR’ + H2O RCOOH + R’OH
Đặc điểm: bội phản ứng thuận nghịch (2 chiều), yêu cầu xúc tác là H2SO4 và nhiệt độ cao.
(vì phản nghịch ứng thuận nghịch cần este vẫn còn dư và sản xuất thành hai chất lỏng → tách bóc lớp )
b/ Thủy phân trong môi trường kiềm: (phản ứng xà phòng hóa)
Ví dụ: CH3COOC2H5 + Na
OH

Tổng quát: RCOOR’ + Na
OH

Đặc điểm: bội nghịch ứng 1 chiều (không thuận nghịch) , xảy ra ở nhiệt độ cao.
(vì bội phản ứng 1 chiều nên este không còn → sản phẩm đồng hóa )
(**) một số trong những phản ứng đặc biệt:
c/ Este bao gồm dạng anđêhit: RCOOCH=CH-R’ (R cùng R’ là H hoặc những gốc hiđrôcacbon)
Khi thủy phân trong môi trường axit: hình thành axit cùng anđêhitVí dụ: CH3COOCH=CH2 + H2O CH3COOH + CH3CHO
Khi thủy phân trong môi trường xung quanh bazơ: hình thành muối cùng anđêhitVí dụ: HCOOCH=CH-CH3 + Na
OH

d/ Este đối kháng chức của phenol: cùng Na
OH hoặc KOH tỉ lệ 1:2, sản phẩm tạo 2 muối và nước.
RCOOC6H4R’ + 2Na
OH → RCOONa + R’C6H4ONa + H2O
Ví dụ: CH3COOC6H5 + 2Na
OH → CH3COONa + C6H5ONa + H2O
HCOOC6H4CH3 + 2Na
OH → HCOONa + CH3C6H4ONa + H2O
e/ Este tráng bạc: có dạng HCOOR (R bất kì)
f/ phản ứng ở cội hiđrôcacbon: những este ko no gồm phản ứng ở gốc hiđrôcacbon (phản ứng cộng dung dịch Br2, phản bội ứng trùng đúng theo …)
g/ phản nghịch ứng cháy: este no đơn hở Cn
H2n
O2 + O2

CO2 + n
H2O
V/ Điều chế:
Các este thường xuyên được điều chế bằng cách đun sôi hỗn hợp ancol và axit cacboxylic, xuất hiện H2SO4 đặc có tác dụng xúc tác (phản ứng este hóa)RCOOH + R’OH RCOOR’ + H2O
Một số este có phương pháp điều chế riêng:Vinyl axetat: CH3COOH + CH≡CH CH3COOCH=CH2
Este của phenol: C6H5OH + (CH3CO)2O → CH3COOC6H5 + CH3COOH
Anhidrit axetic phenyl axetat
VI.Ứng dụng:
Do có khả năng hòa tan tốt nhiều hóa học nên một số este được dùng làm dung môi để tách, chiết chất hữu cơ (etyl axetat), pha sơn (butyl axetat).
Một số polime của este được dùng làm chất dẻo: poli (vinyl axetat), poli (metyl metacrylat)…
Một số este bám mùi thơm, không độc, được dùng làm chất tạo hương thơm trong công nghiệp hoa màu (benzyl fomat, etyl fomat,… ), đồ trang điểm (linalyl axetat, geranyl axetat,…)
BÀI II : LIPIT
I. Khái niệm: Lipit là mọi hợp hóa học hữu cơ có trong tế bào sống, không kết hợp trong nước mà lại tan các trong dung môi hữu cơ không phân cực.
Về khía cạnh cấu tạo, nhiều phần lipit là các este phức tạp, bao hàm chất béo (còn hotline là triglixerit), sáp, steroit cùng photpholipit,…
II. Chất béo:
1. Khái niệm: chất phệ là trieste của glixerol với các axit béo, gọi bình thường là triglixerit hay triaxylglixerol.
Axit khủng là axit solo chức gồm mạch cacbon dài, ko phân nhánh, số C chẵn (từ 12 → 24)
Công thức cấu tạo chung của chất béo :
Trong đó R1 , R2 , R3 là các gốc hiđrocacbon, có thể giống nhau hoặc không giống nhau.
Các axit bự và chất bự thường gặp:
| Axit béo | Chất béo |
| C15H31COOH hoặc (CH3 | (C15H31COO)3C3H5 hoặc C51H98O6: tripanmitin (tripanmitoylglixerol ) (k = 3) |
| C17H35COOH hoặc (CH3 | (C17H35COO)3C3H5 hoặc C57H110O6: tristearin (tristearoylglixerol ) (k = 3) |
| C17H33COOH hoặc (cis CH3 | (C17H33COO)3C3H5 hoặc C57H104O6: Triolein (trioleoylglixerol) (k = 6) |
| C17H33COOH hoặc (cis – CH3 | (C17H33COO)3C3H5 hoặc C57H104O6: Triolein (trioleoylglixerol) (k = 6) |
| C17H31COOH hoặc C18H32O2: axit linoleic (axit không no, 2 nối song C=C, k = 3) | (C17H31COO)3C3H5 hoặc C57H98O6: trilinolein (trilinoleoylglixerol) (k = 9) |
| Với k là tổng số link pi trong hóa học béo |
2. đặc điểm vật lí:
Ở ánh nắng mặt trời thường, chất béo ở tâm lý lỏng hoặc rắn.(C15H31COO)3C3H5 cùng (C17H35COO)3C3H5 là hóa học rắn (mỡ).
(C17H33COO)3C3H5 cùng (C17H31COO)3C3H5 là hóa học lỏng (dầu).
Nhẹ hơn nước, không tan trong nước, nhưng mà tan nhiều trong số dung môi hữu cơ như benzen, hexan, clorofom, …3. đặc thù hóa học
a/ phản ứng thủy phân:
(C17H35COO)3C3H5 + 3H2O 3C17H35COOH + C3H5(OH)3
tristearin axit stearic glixerol
b/ phản nghịch ứng xà chống hóa :
(C17H35COO)3C3H5 + 3Na
OH

tristearin natri stearat glixerol
Vì muối natri stearat làm xà phòng, đề nghị phản ứng này được điện thoại tư vấn là làm phản ứng xà phòng hóa.
c/ phản nghịch ứng cộng hiđro của chất khủng lỏng :
(C17H33COO)3C3H5 + 3H2 (C17H35COO)3C3H5
Phản ứng này được sử dụng trong công nghiệp để đưa hóa chất khủng lỏng (dầu) thành mỡ chảy xệ rắn, thuận lợi cho bài toán vận chuyển hoặc thành bơ tự tạo và để sản xuất xà phòng.
** Dầu mỡ để lâu thông thường có mùi khó chịu (hôi, khét) nhưng mà ta call là hiện tượng kỳ lạ mỡ bị ôi. Tại sao của hiện tượng này là do links đôi C=C ở gốc axit ko no của chất mập bị lão hóa chậm vì chưng oxi trong không gian thành peoxit, hóa học này bị phân bỏ thành các anđêhit tất cả mùi khó chịu và gây hại cho những người ăn. Sau khoản thời gian đã được dùng để làm rán, dầu mỡ cũng bị oxi hóa một trong những phần thành anđêhit, bắt buộc nếu dùng lại dầu mỡ chảy xệ này thì ko đảm đảm bảo sinh bình yên thực phẩm.
4. Vai trò với ứng dụng
Vai trò : thức ăn đặc biệt quan trọng của con người, nguồn hỗ trợ và dự trữ năng lượng, nguyên liệu tổng hợp hóa học hữu cơ khác, bảo đảm an toàn sự di chuyển và hấp thụ những chất hài hòa được trong hóa học béo.
Ứng dụng : pha trộn xà phòng, glixerol, sản xuất thực phẩm. Dầu thực vật → động cơ điezen.
CHƯƠNG 2: CACBOHIĐRAT
I/ Khái niệm: Cacbohiđrat là phần lớn hợp chất hữu cơ tạp chức và thông thường sẽ có công thức phổ biến là Cn(H2O)m .
II/ Phân loại: Cacbohiđrat được chia thành 3 đội sau :
Monosaccarit (đường đơn) : là team cacbohiđrat dễ dàng nhất, cấp thiết thủy phân được. Thí dụ : glucozơ cùng fructozơ.
Đisaccarit (đường đôi) : là team cacbohiđrat nhưng khi thủy phân từng phân tử hiện ra hai phân tử monosaccarit. Ví dụ : saccarozơ, mantozơ.
Polisaccarit (đường đa) : là nhóm cacbohiđrat phức tạp, khi thủy phân cho cùng từng phân tử sinh ra những phân tử monosaccarit. Thí dụ : tinh bột với xenlulozơ.
I. MONOSACCARIT
| GLUCOZƠ | FRUCTOZƠ | |
| I/ đặc điểm vật lí | Chất rắn, tinh thể không màu, dễ dàng tan vào nước, vị ngọt ko ngọt bằng đường mía. – Có đa số trong các thành phần của cây như lá, hoa, rễ,… với nhất là trong trái chín. Bao gồm trong cơ thể người và rượu cồn vật. Có khá nhiều trong quả nho nên gọi là mặt đường nho. Trong mật ong : khoảng chừng 30%, trong máu fan : nồng độ không đổi khoảng tầm 0,1%. | Chất kết tinh, ko màu, dễ tan vào nước, gồm vị ngọt hơn mặt đường mía, có tương đối nhiều trong quả ngọt như xoài, dứa ,… Đặc biệt vào mật ong gồm tới 40% fructozơ tạo nên mật ong gồm vị ngọt sắc. |
| Ii/ kết cấu phân tử | Dạng mạch hở : – Dữ kiện thực nghiệm xác định cấu trúc của glucozơ : + Glucozơ có phản ứng tráng bạc và bị oxi hóa vày nước brom chế tạo ra thành axit gluconic, minh chứng phân tử tất cả nhóm CHO. + Glucozơ tác dụng Cu(OH)2 ngơi nghỉ t0 thường, mang lại dd xanh lam, chứng tỏ glucozơ có tương đối nhiều nhóm OH tại vị trí kề nhau. + Glucozơ sản xuất este cất 5 nơi bắt đầu axit CH3COO chứng tỏ phân tử tất cả 5 đội OH. + Khử trọn vẹn glucozơ chiếm được hexan, minh chứng có 6 nguyên tử C vào phân tử glucozơ sản xuất thành một mạch không nhánh. Vậy : Glucozơ là hợp hóa học tạp chức, có 5 nhóm OH cùng anđêhit đơn chức. CTCT : CH2OH-CHOH-CHOH-CHOH-CHOH-CH=O hoặc CH2OH * Dạng mạch vòng : tồn tại chủ yếu ở cả hai dạng mạch vòng 6 cạnh : α – glucozơ với β – glucozơ. | Dạng mạch hở : Là hợp hóa học tạp chức bao gồm 5 nhóm OH cùng 1 đội xeton. CH2OH–CHOH– CHOH–CHOH– CO–CH2OH *Dạng mạch vòng : tồn tại đa số 2 dạng vòng 5 cạnh α – fructozơ và β – fructozơ. |
| IV/ Điều chế và ứng dụng | 1. Điều chế: Trong công nghiệp, glucozơ được điều chế bằng phương pháp : + Thủy phân tinh bột, xúc tác axit clohiđric loãng hoặc enzim. + Thủy phân xenlulozơ (trong vỏ bào, mùn cưa,…) , xúc tác HCl đặc hoặc H2SO4 đặc 2. Ứng dụng: + Là chất dinh dưỡng, có tác dụng thuốc tăng lực cho tất cả những người già, trẻ em và tín đồ ốm. + dùng để làm tráng gương, tráng ruột phích, nguyên liệu sản xuất ancol etylic … | + Saccarozơ là thực phẩm đặc biệt quan trọng của con người. + trong công nghiệp hoa màu : là nguyên liệu để gia công bánh kẹo, nước giải khát, đồ dùng hộp. + vào công nghiệp dược phẩm : được dùng làm pha thuốc. + Là nguyên liệu để thủy tạo thành glucozơ với fructozơ sử dụng trong kĩ thuật tráng gương, tráng ruột phích. |
| III. đặc điểm hóa học | 1. Tính chất của ancol đa chức: a/ chức năng với Cu(OH)2: Ở ánh sáng thường, glucozơ phản ứng với Cu(OH)2 mang đến phức đồng glucozơ (C6H11O6)2Cu màu xanh da trời lam (tương từ bỏ glixerol). 2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2H2O b/ bội nghịch ứng chế tác este : Glucozơ có thể tạo este chứa 5 cội axit axetic trong phân tử khi thâm nhập phản ứng cùng với anhiđrit axetic (CH3CO)2O, có mặt piriđin. 2. đặc thù của anđehit : a/ lão hóa glucozơ bằng dung dịch Ag Dung dịch Ag HOCH2 b/ thoái hóa glucozơ bởi Cu(OH)2: Trong môi trường thiên nhiên kiềm, Cu(OH)2 thoái hóa glucozơ tạo thành muối hạt natri gluconat, đồng (I) oxit cùng H2O . HOCH2 c/ Khử glucozơ bởi hiđro: CH2OH (sobitol) 3. Bội nghịch ứng lên men : C6H12O6 → 2C2H5OH + 2CO2 ↑ | + tương tự như glucozơ, fructozơ tính năng với Cu(OH)2 cho dung dịch phức (C6H11O6)2Cu màu xanh lá cây lam (tính hóa học của ancol nhiều chức), cộng hiđro cho poliancol C6H14O6 (tính chất của tập thể nhóm cacbonyl). + giống như glucozơ, fructozơ bị oxi hóa do dung dịch Ag |
| IV. Điều chế cùng ứng dụng | 1. Điều chế: vào công nghiệp, glucozơ được điều chế bằng phương pháp : + Thủy phân tinh bột, xúc tác axit clohiđric loãng hoặc enzim. + Thủy phân xenlulozơ (trong vỏ bào, mùn cưa,…) , xúc tác HCl sệt hoặc H2SO4 đặc 2. Ứng dụng: + Là hóa học dinh dưỡng, có tác dụng thuốc tăng lực cho tất cả những người già, trẻ nhỏ và tín đồ ốm. + dùng để làm tráng gương, tráng ruột phích, vật liệu sản xuất ancol etylic …
| 1. Điều chế: trong công nghiệp, glucozơ được điều chế bằng cách : + Thủy phân tinh bột, xúc tác axit clohiđric loãng hoặc enzim. + Thủy phân xenlulozơ (trong vỏ bào, mùn cưa,…) , xúc tác HCl sệt hoặc H2SO4 đặc 2. Ứng dụng: + Là hóa học dinh dưỡng, làm thuốc tăng lực cho tất cả những người già, trẻ nhỏ và người ốm. + dùng để tráng gương, tráng ruột phích, vật liệu sản xuất ancol etylic … Trong nội dung bài viết này, cdvhnghean.edu.vn vẫn gửi đến những em phiên bản tổng hợp lý thuyết Hóa 12 học kì 1 ko thể không hề thiếu hơn. Các em hoàn toàn có thể nhìn lại rất nhiều phần trung tâm nhất để khắc sâu kiến thức.  Tính đến thời gian hiện tại, teen 2K1 đã từng đi được nửa chặng đường. Trước mắt những em chỉ từ một học tập kì nữa thôi là chúng ta sẽ bước vào kì thi thpt Quốc gia. Trong các số ấy môn hóa học là môn bao gồm số thắc mắc về triết lý chiếm tới 60%. Phạm vi kỹ năng và kiến thức của đề thi thpt QG 2019 lại không ngừng mở rộng ra cả 3 lớp 10, 11 với 12. Các em sẽ yêu cầu thật sự cố gắng để ghi nhớ tương đối đầy đủ kiến thức. Nhưng new chỉ học không còn học kì 1 nhưng mà lượng kiến thức và kỹ năng Hóa 12 đã vô cùng "đồ sộ". Làm thế nào để tổng hợp ngắn gọn, dễ nhớ và rất có thể học lại bất cứ khi nào cần? Bản tổng hợp triết lý Hóa 12 học tập kì 1 tương đối đầy đủ nhấtcdvhnghean.edu.vn gọi được rằng, tiết kiệm được thời gian học là mong muốn của hàng tỷ nghìn teen 2K1. Chính vì như thế cdvhnghean.edu.vn sẽ giúp các em tổng hợp kim chỉ nan Hóa 12 học kì 1 khôn cùng ngắn gọn, khôn xiết dễ nhớ. Trước tiên chúng ta sẽ điểm lại các kiến thức Hóa học giữa trung tâm mà các em đã làm được học ở học kì I. Lý thuyết Hóa 12 học kì I tuyệt nhất định đề xuất nhớĐại cương sắt kẽm kim loại là phần kỹ năng và kiến thức Hóa học trung tâm nhất mà lại teen 2K1 buộc phải ghi lưu giữ sau học tập kì I. Ở phần này, học viên sẽ cần nhớ vớ tần thật các yếu tố sau: - địa chỉ của sắt kẽm kim loại trong bảng tuần hoàn. - cấu tạo của kim loại. - tính chất vật lí. - đặc thù hóa học. - dãy điện hóa của kim loại. - Sự làm mòn kim loại. - Các cách thức điều chế kim loại. Tổng hợp định hướng Hóa 12 học tập kì 1 qua InfographicInfographic là 1 dạng vật họa tin tức trực quan lại đã được dùng từ vô cùng lâu. Trên cầm cố giới, người ta thường xuyên ưu tiên sử dụng infographic nhằm truyền cài đặt thông tin, kiến thức và kỹ năng nhanh chóng.Bởi vì Infographic sử dụng hình ảnh để diễn tả nội dung truyền đạt một cách ngắn gọn và dễ hiểu. Tín đồ đọc ko cần mất nhiều thời gian vẫn hoàn toàn có thể nắm bắt tức thì được thông tin. Chính bởi vậy, đề giúp học sinh hiểu sâu, nhớ lâu được các bài chất hóa học trừu tượng, cdvhnghean.edu.vn đã thực hiện Infographic. Bài học mà các em thấy phức tạp, dài lê giờ đây chỉ gói gọn gàng trong một vài trang giấy các hình ảnh bắt mắt nhưng vẫn chứa được khá đầy đủ thông tin. Sau đây là phần tổng hợp triết lý Hóa 12 học tập kì 1 bằng Infographic của cdvhnghean.edu.vn.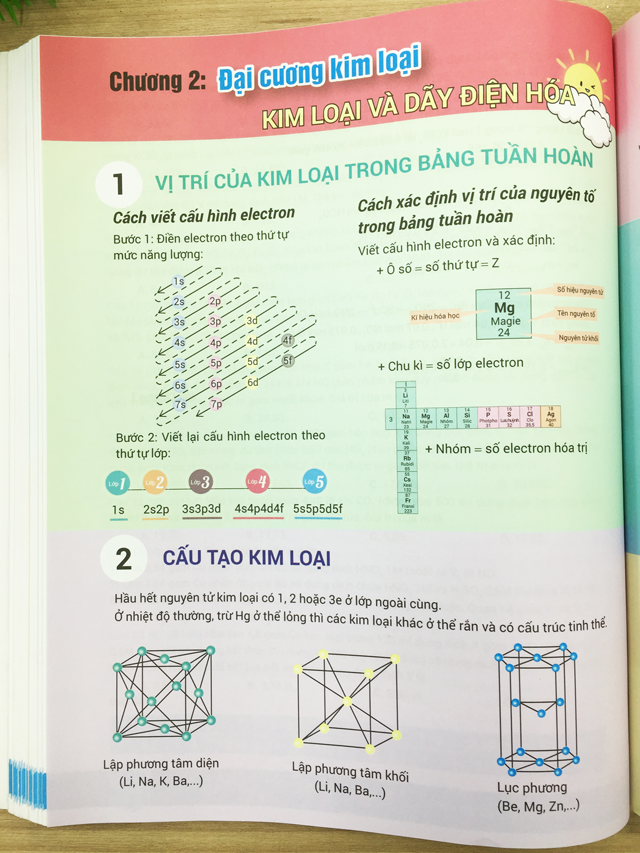  Các em hoàn toàn có thể thấy lượng chữ viết nhưng mà mình bắt buộc học thuộc đã được giảm tải buổi tối đa. Cầm cố vào đó là cách trình bày logic, rõ ràng, ngắn gọn và dễ hiểu.  Chỉ chần phát âm lướt qua, những em đã rất có thể nhớ được nội dung cụ lõi của bài học. Như vậy, việc ghi nhớ kỹ năng và kiến thức sẽ trở bắt buộc vô thuộc nhàn nhã. Em sẽ có tương đối nhiều thời gian nhằm ôn tập môn học tập khác cũng giống như luyện đề thành thục hơn. Để tham khảo cụ thể hơn về phần tổng hợp định hướng Hóa học 12 học kì một phần Điều chế kim loại, các em hãy xem thêm cuốn Infographic đoạt được kỳ thi THTP nước nhà môn Hóa học. Cuốn sách trước tiên trên thị phần tổng hợp núi kiến thức 3 năm chỉ trong một cuốn sách bằng Infographic. Với cuốn sách luyện thi THPT giang sơn mô Siêu tuyệt kỹ hiểu sâu ghi nhớ lâu kiến thức và kỹ năng 3 năm- núm trọn điểm 9, 10 Infographic chinh phục kỳ thi THPT giang sơn môn chất hóa học được ca ngợi là siêu bí quyết giúp teen 2K1 hạ gục triết lý 3 năm, ẵm điểm 9, 10. Kiến thức và kỹ năng được xung khắc sâu mang đến tận ngày thi. Không chỉ tất cả cách trình diễn kiến thức khoa học, sách còn hệ thống lượng bài bác tập rất chất. Tuyển tập thắc mắc trích từ bỏ đề thi thật, thi test THPT tổ quốc của trường chuyên, lớp chọn.100% ví dụ minh họa vào cuốn sách luyện thi THPT đất nước môn hóa học này được trích từ bỏ đề thi thật, thi demo THPT đất nước của Bộ, những trường chuyên lớp chọn. Bài tập được phân dạng đầy đủ chủ yếu ở mức vận dụng và vận dụng cao. Tất cả phân tích, phía dẫn ví dụ giúp em nâng cấp khả năng bốn duy nhanh.  Bên cạnh kia sách còn kèm theo những tiện ích technology hỗ trợ tối đa tác dụng học tập. + đoạn clip bài giảng do tác giả trực tiếp ghi hình, giảng giải đến em những phần câu chữ khó. Đồng thời thầy cô cũng giải mẫu mang đến em những dạng câu hỏi khó mang đến cực khó. + hệ thống thi test trực con đường CCTest nhằm em rèn luyện thành thục đông đảo dạng bài, có tác dụng quen với cấu trúc đề thi thật. + giáo viên miễn phó 24/24. Lúc nào em chạm mặt khó khăn trong quy trình học rất có thể đăng câu hỏi lên nhóm cung ứng của cdvhnghean.edu.vn. Thầy cô với các cả nhà sinh viên xuất sắc sẽ giải đáp cho các em ngay. Cuốn sách tuyệt đối hoàn hảo để em giành vững chắc tấm vé vào trường đh Top đầuGiúp em tổng hợp triết lý Hóa 12 học tập kì 1 chỉ là 1 trong chuyện nhỏ. Infographic chinh phục kỳ thi THPT đất nước môn Hóa học còn là một trợ thủ đắc lực để em giành có thể tấm vé vào trường đại học top đầu. |